欧盟UDI新规出台!眼镜架、镜片及老花镜标识管理迎来重大变革
面对海量产品变体带来的UDI标识难题,欧盟为高度个性化器械找到了新解决方案。
原文链接:https://eur-lex.europa.eu/eli/reg_del/2025/1920/oj

近日,欧盟官方期刊(OJ EU)发布了《欧盟委员会授权法规(EU)2025/1920》,对《医疗器械法规 (EU) 2017/745》(MDR)中关于眼镜框架、眼镜镜片和即戴式老花镜的唯一器械标识(UDI)要求进行了重要修订。
这一新规旨在解决这类高度个性化产品因参数组合繁多而导致的UDI标识管理难题,为企业提供了更高效的合规路径。
1、新规背景:高度个性化器械的 UDI 困境
欧盟为强化医疗器械的可追溯性,引入了唯一器械标识(UDI)系统。该系统要求制造商在将器械投放市场前,为其分配唯一器械标识。
UDI由器械标识符(UDI-DI)和生产标识符(UDI-PI)构成。其中,UDI-DI是用于识别特定型号器械和制造商的核心要素,需在欧盟医疗器械数据库(Eudamed)中注册。
然而,眼镜框架、眼镜镜片和即戴式老花镜等产品由于存在大量的设计参数和结构变体,同一型号下可能衍生出海量UDI-DI。按照原有规则,每个产品变体都需单独分配 UDI-DI,导致同类眼镜产品的 UDI-DI 数量激增。
这种个体化管理方式导致数据库冗余条目激增,给制造商和监管机构带来了沉重负担。
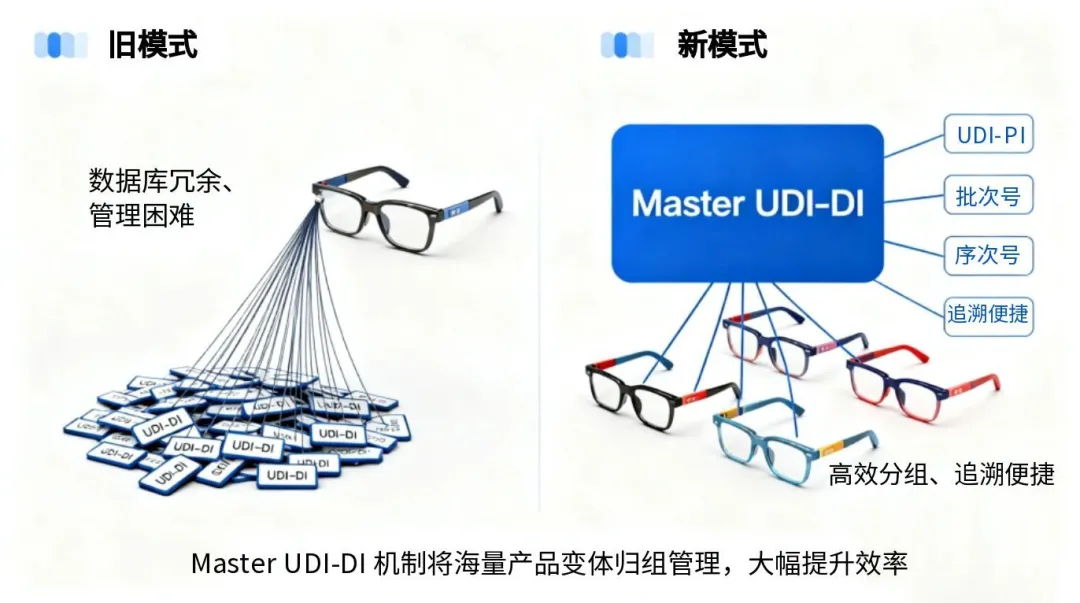
2、解决方案:Master UDI-DI 机制
为解决这一问题,欧盟引入了 “Master UDI-DI” 机制,允许将设计参数相似的器械归组在同一个主标识符下。
与传统 UDI-DI(1个型号对应1个码)不同,Master UDI-DI是1组相似产品对应1个主码,再通过生产批号、序列号等来区分单品。
这种分组方式大幅减少了数据库的冗余,提高了管理效率,也使得相关产品的追溯更加便捷。
3、具体产品要求
新法规在《欧盟医疗器械法规(EU)2017/745》附件 VI 的 C 部分新增 “6.6.2” 章节,明确眼镜框架、镜片、即戴式老花镜的 UDI-DI 分配规则,核心是 “相同设计参数组合的产品,共用 1 个 Master UDI-DI”,具体要求如下:

-
眼镜框架(Spectacle frames):
共用 Master UDI-DI 的条件:具有相同设计参数组合的眼镜框架,将被分配同一个 UDI-DI(即 “主 UDI-DI”),设计参数中至少需包含水平盒装镜片尺寸。
变更要求:除遵循原法规第 3.9 节的要求外,一旦上述设计参数组合发生变化,就需要重新分配新的 “主 UDI-DI”。
-
眼镜镜片(Spectacle lenses):
共用 Master UDI-DI 的条件:相同设计参数组合的眼镜片共用一个 “主 UDI-DI”,设计参数至少涵盖平均球面度数(等效球镜度数)组、附加度数组以及相似视力损伤类型组。
变更要求:若上述设计参数组合出现变动,需按照规定重新申请新的 “主 UDI-DI”,同时需符合原法规第 3.9 节的相关要求。
-
即戴式老花镜(Ready-to-wear Reading Spectacles):
共用 Master UDI-DI 的条件:对于即戴式老花镜,具有相同设计参数组合(至少包含水平盒装镜片尺寸和镜片球面度数)的产品,可共用一个 “主 UDI-DI”。
变更要求:当设计参数组合发生改变时,需重新分配 “主 UDI-DI”,且需满足原法规第 3.9 节的要求。
-
需特别注意:上述规则是在原法规 “3.9 章节” 要求的基础上新增的补充条件,并非替代原有合规要求 —— 企业仍需遵守 UDI 载体(如条形码、二维码)的印刷、扫描标准,以及 UDI 数据上传 Eudamed 的时限要求。
4、适用时间及范围
(一)适用时间
法规将于2028年11月1日正式适用。企业可在此日期前自愿采用新机制,以便提前完成系统对接与EUDAMED注册调整。
新法规明确了两个关键时间点,相关企业需重点关注:
1.生效时间:法规将在欧盟官方期刊发布后的第 20 天正式生效(即 2025 年 10 月中旬左右);
2. 实施时间:2028 年 11 月 1 日起,所有在欧盟市场上市的眼镜框架、镜片及即戴式老花镜,必须按新规则分配 Master UDI-DI;
3. 提前合规窗口:法规允许制造商在 2028 年 11 月 1 日前,提前按照新规则分配 Master UDI-DI,为企业预留了充足的系统调整时间。
(二)适用范围与法律效力
该法规在欧盟及EEA成员国直接适用,无需成员国再行立法。涉及产品出口欧盟的制造商、授权代表、进口商及经销商,均应在2028年前完成相应调整。

5、给企业的建议
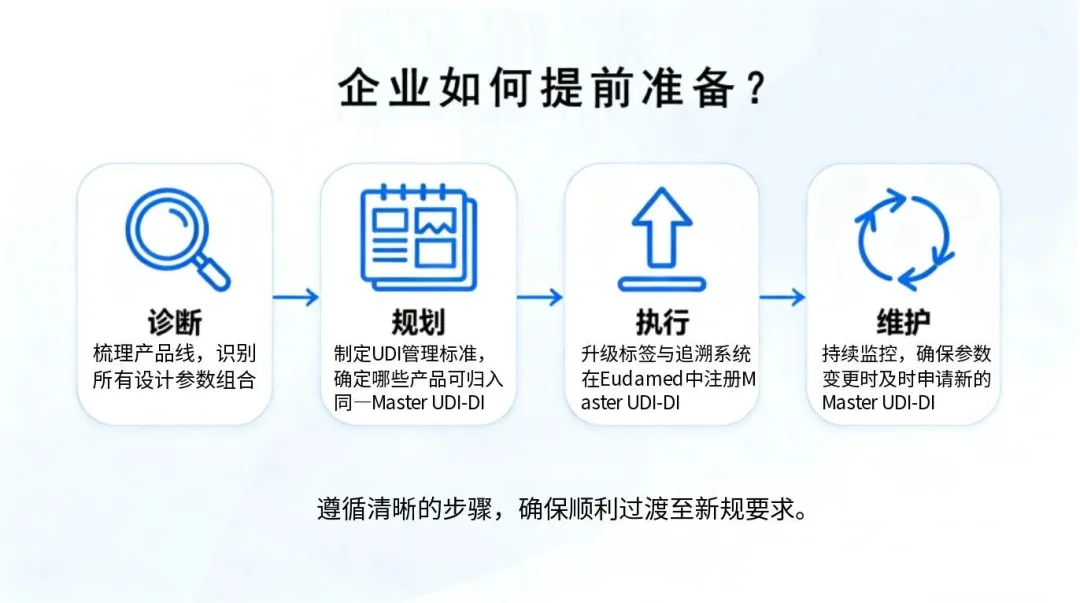
面对这一新规,相关医疗器械企业(尤其是眼镜及光学产品制造商、出口商)应积极准备,以确保顺利过渡:
-
密切关注法规动态:及时关注法规批准和生效进程,确保及时了解最新要求。
-
完善内部管理和追溯体系:制定相关管理 UDI标准,升级内部系统,适配 Master UDI-DI 管理,对产品的设计参数组合等信息进行准确记录和管理,以便生产、物流等各个环节能够快速、准确地分配和更新 Master UDI-DI。
-
提前规划合规工作:虽然眼镜类产品的截止期至2028年,但建议企业提前同步启动数据库注册。官方强烈推荐企业利用自愿分配期提前申请 Master UDI-DI。
-
标签设计双重适配:在进行标签设计时,要充分考虑新规要求,做到双重适配,既满足 Master UDI-DI 的标识规范,又符合其他相关法规对标签的要求。
提前准备是应对新规的关键。虽然眼镜类产品 Master UDI-DI 的强制实施截止日期是2028年11月,但官方强烈推荐企业利用自愿分配期提前申请。
尽早规划合规路径,不仅能确保产品在欧盟市场的顺利流通,也能借此机会优化内部管理体系,提升市场竞争力。
Kiwa 医疗健康服务
Kiwa 是欧盟医疗器械法规(REGULATION (EU) 2017/745,简称“MDR”)下指定公告机构 NB 1984。
|
公告机构号 |
公告机构名称 |
国家 |
国家 |
|
NB 1984 |
Kiwa Belgelendirme Hizmetleri A.Ş. |
Türkiye |
土耳其 |
|
NB 1912 |
Kiwa Assurance B.V. |
Netherlands |
荷兰 |
|
NB 0476 |
KIWA CERMET ITALIA S.P.A. |
Italy |
意大利 |
* 数据来源:欧盟NANDO (New Approach Notified and Designated Organizations) 数据库。
· 欧盟 CE MDR 认证:全面覆盖低中高风险及有源、无源医疗器械产品。
· ISO 13485 体系认证:UKAS 国际权威认可,提升质量管理体系竞争力,助力企业高效合规。
电话:400-016-9000
邮箱:post@bcc.com.cn
联系地址:北京市东城区广渠门内大街45号D座5层



 京公网安备11010102007586号
京公网安备11010102007586号